中科大金腾川团队发现SARS-CoV-2 Spike Y453F变异株通过表位突变逃逸CD8+ T细胞免疫的分子机制
2024年8月5日,中国科学技术大学金腾川团队在Journal of biological chemistry 杂志在线发表题为“Structural insights into immune escape at killer T cell epitope by SARS-CoV-2 Spike Y453F variants”的研究性论文。

由主要组织相容性复合体(MHC,在人类中又被称为HLA)和T细胞受体(TCR)介导的CD8+ T细胞免疫在提供免疫记忆和抗病毒感染中起着关键作用。SARS-CoV-2变异株对现有疫苗的保护效力构成了严重挑战。目前,虽然大量与CD8+ T细胞免疫逃逸相关的新冠突变已经被报道,但大多数突变对表位特异性TCR识别的分子效应仍未被探索。在本研究中,我们以HLA-A24限制性NYN 表位(Spike448-456:NYNYLYRLF)为例,探究了表位突变对抗原提成复合物形成的影响。作者发现在该表位上存在四个自然突变,分别是N450K、L452Q、L452R 和Y453F。研究结果表明,这些突变对细胞表面HLA呈递表位的影响很小,但却显著降低了肽-HLA(pHLA)与NYN肽特异性TCR之间的亲和力,尤其是L452R和Y453F突变。此外,作者还解析了负载Y453F肽(NYNYLFRLF)的Y453F-HLA-A24、以及负载野生型肽(NYNYLYRLF)的TCRNYN-I-NYN-HLA-A24三元复合物的晶体结构。结构分析表明,尽管HLA能有效呈递Y453F突变肽,但由于突变肽与表位特异性TCR之间的相互作用减少,破坏了TCR-pMHC抗原复合物的形成,继而逃避CD8+ T 细胞免疫,这是病毒实现细胞免疫逃逸所使用的有效策略之一。
作者通过SPR发现,NYN表位突变降低了其pHLA和特异性TCR之间的亲和力,尤其是L452R和Y453F突变,显著削弱甚至废除了TCR: pHLA之间的相互作用(图1A-F)。此外,尺寸排阻色谱(SEC)的结果表明TCRNYN-I、TCRNYN-II能够与WT-HLA、N450K-HLA和L452Q-HLA形成复合物,但却不能与L452R-HLA和Y453F-HLA突变体蛋白形成TCR-pHLA复合物(图1G-H)。这些结果表明,与L452R和Y453F突变不同,在平均水平上,N450K和L452Q突变是可耐受的。TCR: pHLA相互作用的急剧减少使得肽特异性CD8+ T细胞的TCR受体对L452R和Y453F突变肽的识别效率大大降低,这也与L452R和Y453F显性变异株在逃避HLA-A24限制性细胞免疫中的作用相一致。
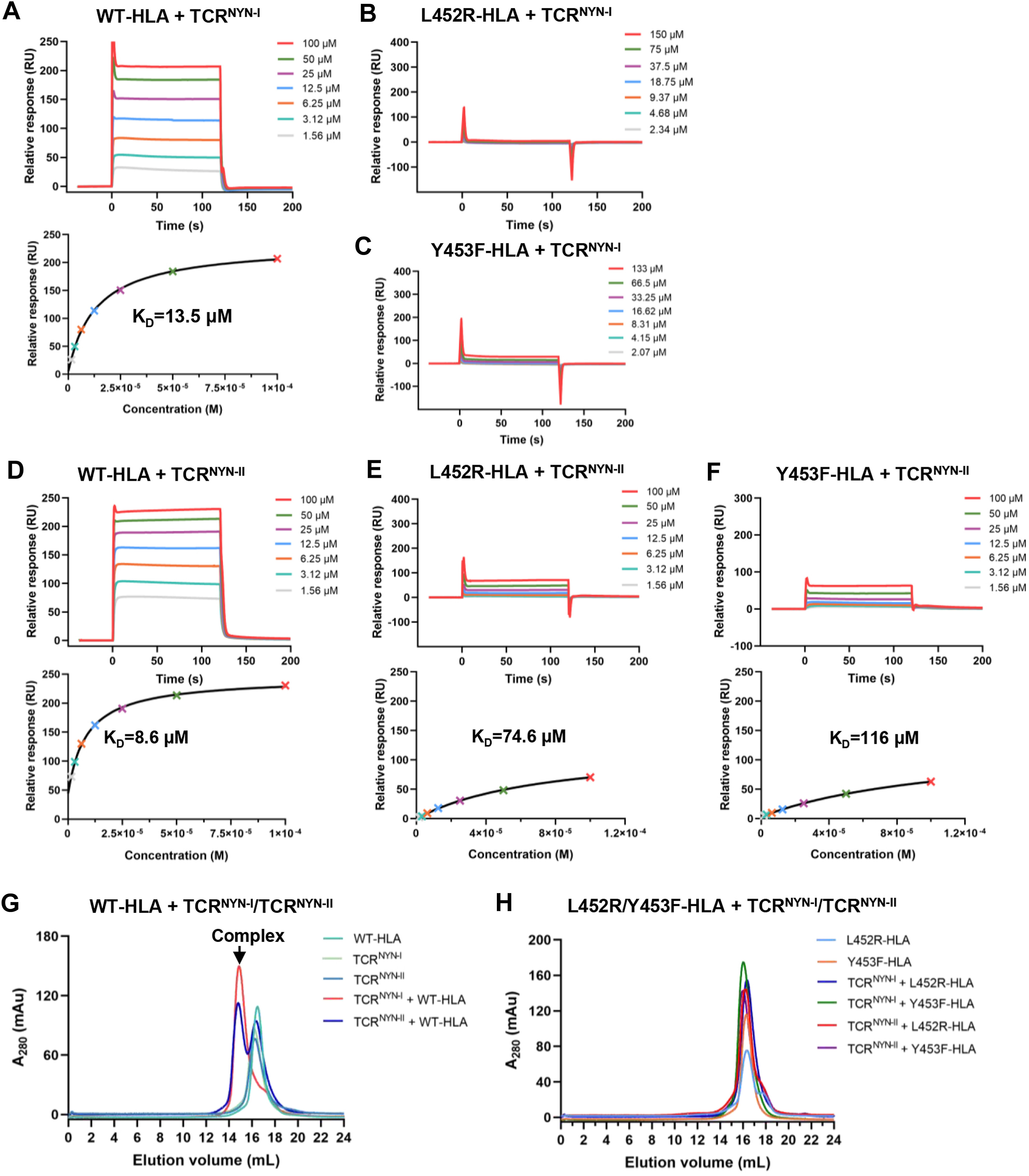
图1. L452R和Y453F突变导致TCR: pHLA相互作用显著降低
然后,作者解析了负载Y453F突变肽(NYNYLFRLF)的Y453F-HLA-A24晶体结构。与之前所解析的装载野生型肽的NYN-HLA-A24结构相比,Y453F突变肽的构象发生了巨大的变化(图2A-C)。有趣的是,与野生型肽相比,Y453F肽与HLA-A24螺旋形成了更多的氢键相互作用(图2D-E)。不仅如此,与WT-HLA相比,L452R-HLA和Y453F-HLA突变体蛋白表现出更高的稳定性(图2F)。这与先前一些研究中所提出的MHC-I类分子与某些突变肽结合减少或消除相反,该结果表明L452R和Y453F突变实际上促进了多肽与HLA-A24抗原结合槽的稳定结合。
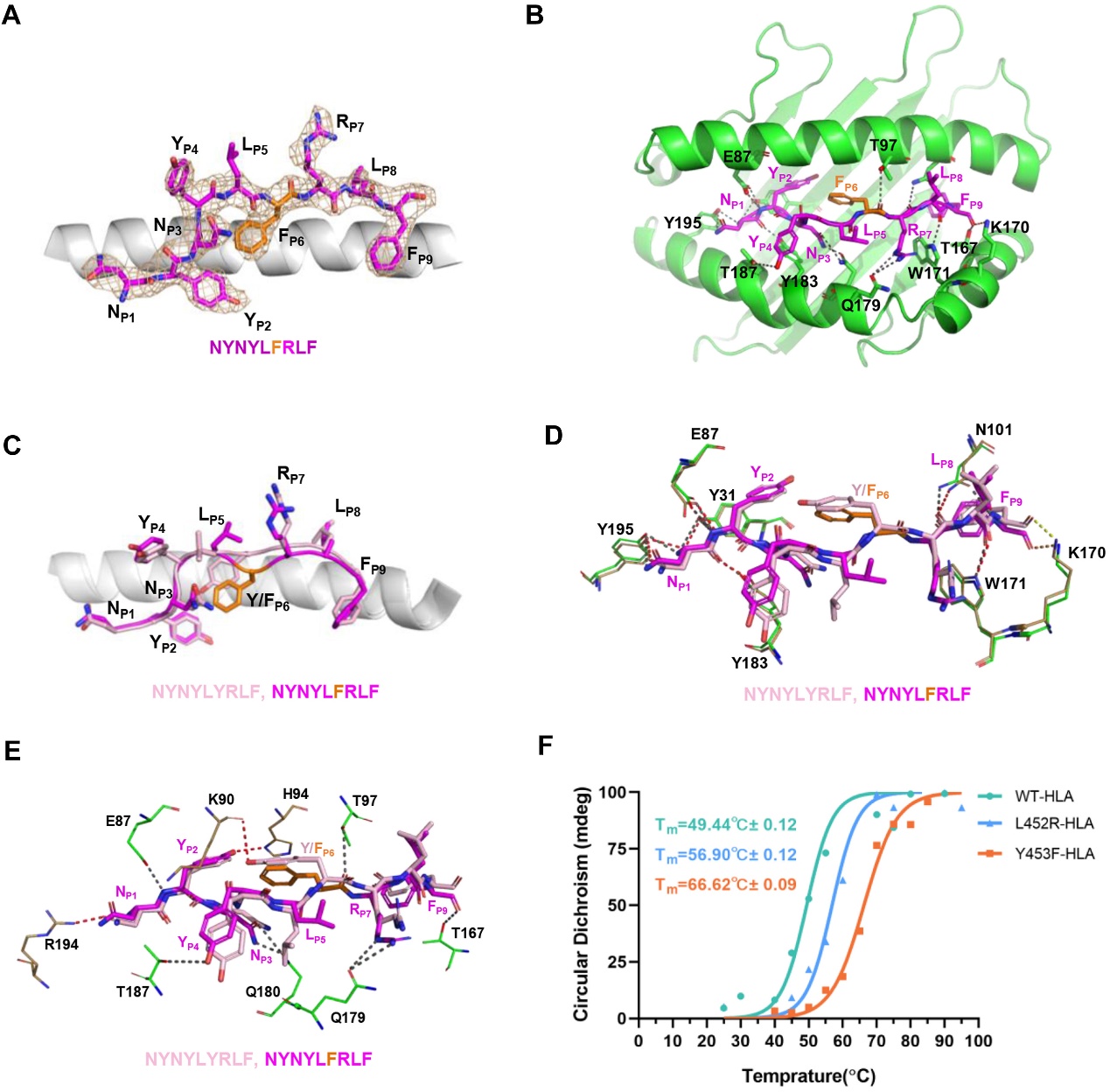
图2. Y453F-HLA-A24与WT-HLA-A24的晶体结构分析
为了深入了解NYN特异性TCR识别的分子基础,作者进一步解析了TCRNYN-I-NYN-HLA-A24(NYNYLYRLF)三元
合物的晶体结构。结构分析表明,TCRNYN-I通过CDR1α和CDR3α与肽的N端建立接触,而CDR3β环主要与C端建立接触(图3A)。TCRNYN-I与NYN肽之间的接触是由CDR1α和CDR3介导的,其中CDR1α、CDR3α和CDR3β分别贡献了32%、27%和41%(图3B)。其中,多肽的P4-Tyr、P5-Leu、P6-Tyr和P7-Arg残基在TCRNYN-I结合过程中发生了构象转移(图3C)。对NYN肽与CDR结合的进一步分析显示,P4-Tyr、P6-Tyr和P7-Arg分别占相互作用的39%、27%和21%,证实了这些残基对TCR识别的重要性(图3D)。其中,P4-Tyr和P7-Arg主要与CDR1α和CDR3β相互作用,分别在结合界面锚定肽的N端和C端(图3E)。主要的焦点是P6-Tyr,CDR1α、CDR3α和CDR3β均与该肽残基形成了广泛接触(图3F)。Y453F-HLA-A24与TCRNYN-I-NYN-HLA-A24复合物的结构比对显示,Y453F变体中的疏水苯丙氨酸可能破坏了原始酪氨酸与TCRNYN-I的接触网络,包括其与CDR之间形成的原始氢键(图3F)。这些结构数据阐明了表位内的显性突变,包括Y453F和L452R,如何破坏CDR环和肽之间的相互作用,进而导致TCRNYN-I T细胞失去识别。
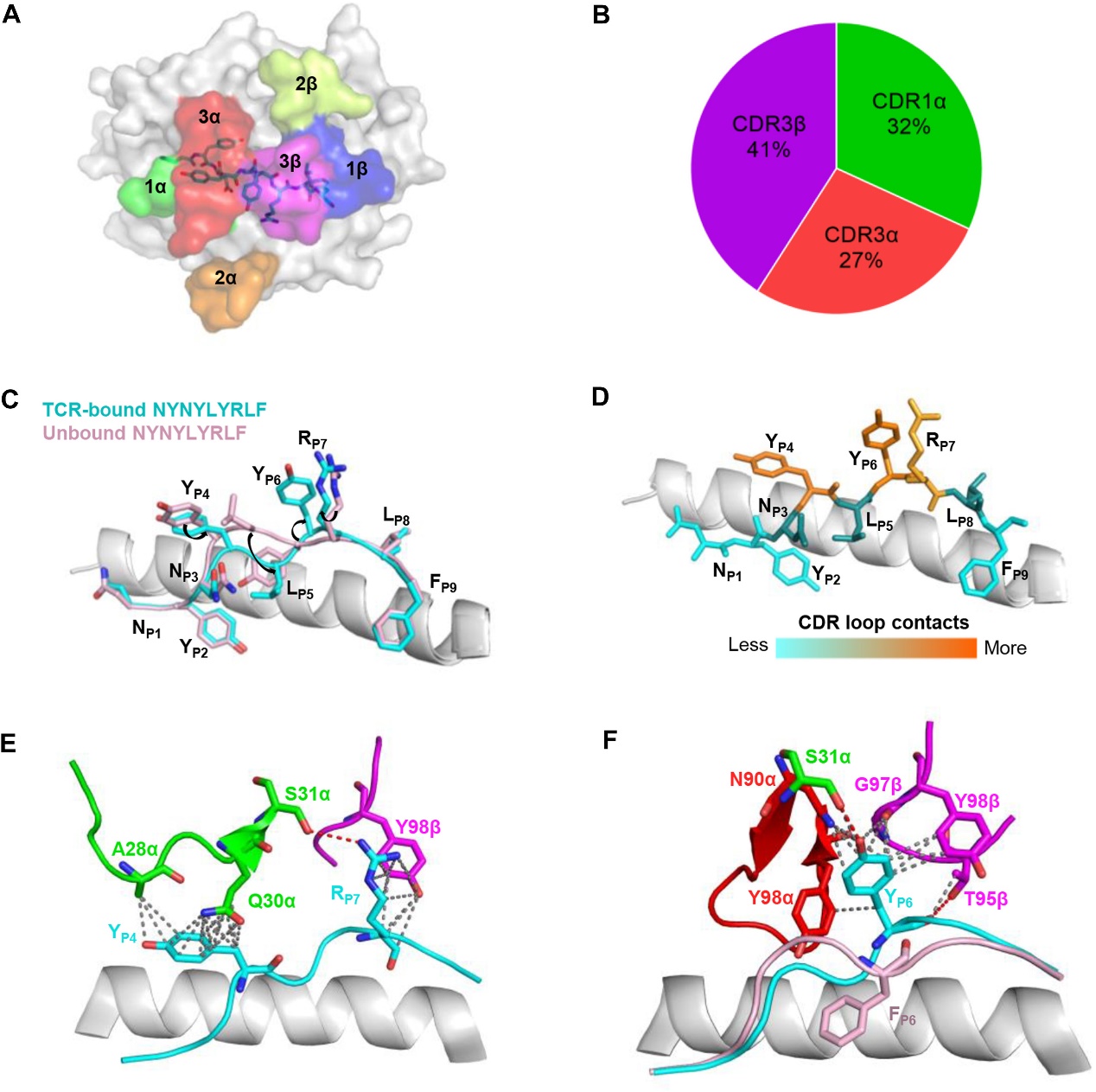
图3. TCRNYN-I与NYN多肽之间的相互作用分析
该工作验证了致病性病毒(SARS-CoV-2)逃避宿主CD8+ T细胞免疫反应的策略。虽然在某些变异中,病毒宿主细胞进入、抗原加工和表位呈递不受影响,但由于突变导致多肽的细微构象变化减少甚至废除了由TCR识别所介导的CD8+ T细胞活化。该研究丰富了我们对病毒突变及其进化驱动力的理解,可能有助于指导未来针对SARS-CoV-2和其他病毒性病原体的疫苗设计和治疗干预。
该工作得到了中科院先导基金、国家自然科学基金、安徽省自然科学基金及中央高校基础研究项目的支持。

